Иммунная система содержит множество средств для борьбы с бактериями. Среди них есть одно, которое заслуживает отдельного внимания в силу весьма интересного и необычного механизма — это так называемые ДНК-сети, которые создают нейтрофилы. Последние представляют собой одну из разновидностей лейкоцитов, причем наиболее распространенную в организме. Они, можно сказать, всегда стоят на страже — первыми встречают противника в лице вирусов, и наносят ему удар всевозможными токсинами. Как правило, сами они гибнут, но предварительно из собственного ядра выпускают свою ДНК, причем закрепляет нить на подходящем субстрате, после чего “отползают”. В результате за ними тянется и распускается нить. В этот момент происходит самое интересное — другие клетки, натыкающиеся на эту нить, начинают от нее плести сеть, используя свою ДНК. В итоге ДНК-сеть нейтрофилов заполняет собой клеточную цитоплазму. Она представляет собой самую настоящую ловушку, выполняющую такую же функцию, как паутина у пауков — задерживает бактерии и передает сигналы макрофагам, которые приползают по тканям и поедают бактерии. Причем, после поедания бактерий они не погибают, а продолжают искать новые жертвы, запутавшиеся в сети. Вместе с тем макрофаги выделяют сигнальные белки, провоцирующие воспалительный процесс и призывающие на помощь другие клетки.
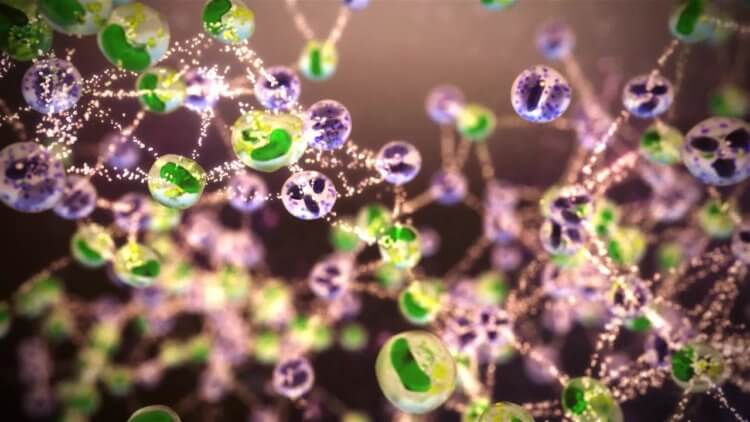
Нейтрофилы способны плести «паутину», чтобы ловить бактерии
Нейтрофилы и макрофаги — как работает сплоченная иммунная система человека
Когда макрофаги работают в паре с Нейтрофилами, они не просто съедают попавших в ДНК-сеть бактерий, а выкусывают их, поглощая при этом и часть самой ДНК. Как заметили во время исследования ученые Университета Вандербильта, потребление микробов вместе с ДНК-сетью имеет свое практическое значение. Дело в том, что в цитоплазме на ДНК-сеть оседают антибактериальные белки. Когда макрофаги поедают вирусы, антибактериальные белки на сети смешиваются с антибактериальными белками самих макрофагов. Это позволяет им более эффективно “переваривать” микробов и не погибать после их поедания. Поэтому, когда макрофаги работают вместе с нейтрофилами, они гораздо эффективнее уничтожают бактерии, чем по одиночке. Детали исследования ученые описывают в своей статье, опубликованной в Science.
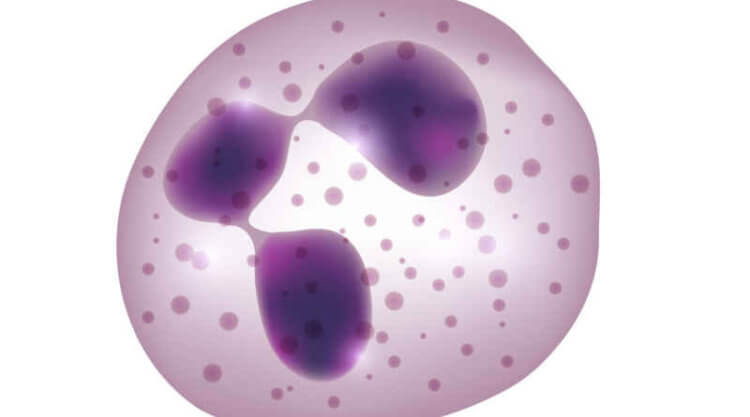
Нейтрофил, который даже после своей гибели борется с бактериями
Также ученым удалось обнаружить белок, который влияет на создание нейтрофилами ДНК-сетей, он имеет название S100A9. Когда в нейтрофилах количество этого белка сокращается, запускается процесс, в результате которого нейтрофильи митохондрии выделяют большое количество кислородных радикалов, то есть агрессивных молекул-окислителей. Правда, митохондрии, которые являются энергетическими органоидами клетки, и сами по себе всегда генерируют радикалы, представляющие собой побочный продукт энергетических реакций. Однако, когда количества белка S100A9 уменьшается, радикалов становится намного больше. Это приводит к тому, что нейтрофилы быстро саморазрушается. При этом, как я сказал выше, нейтрофил выбрасывает из себя ДНК-нить, основу для будущей сетки.
Соответственно, чем меньше у нейтрофилов белка S100A9, тем они быстрее создают ловушку для бактерий из своих нитей ДНК. В результате более эффективно начинают работать макрофаги.
Еще больше материалов о захватывающих открытиях и исследованиях ученых вы найдете на нашем Яндекс.Дзен-канале. Обязательно подпишитесь, чтобы не пропустить.
Аутоимунные заболевания и золотистый стафилококк
Ученые исследовали работу иммунной системы на устойчивом к антибиотикам золотистом стафилококке (MRSA), а также других некоторых бактериях. При этом авторы работы заметили, что повышенное количество белка S100A9 содержится у людей, имеющих аутоиммунные заболевания, к которым относится красная волчанка, а также и ревматоидный артрит.
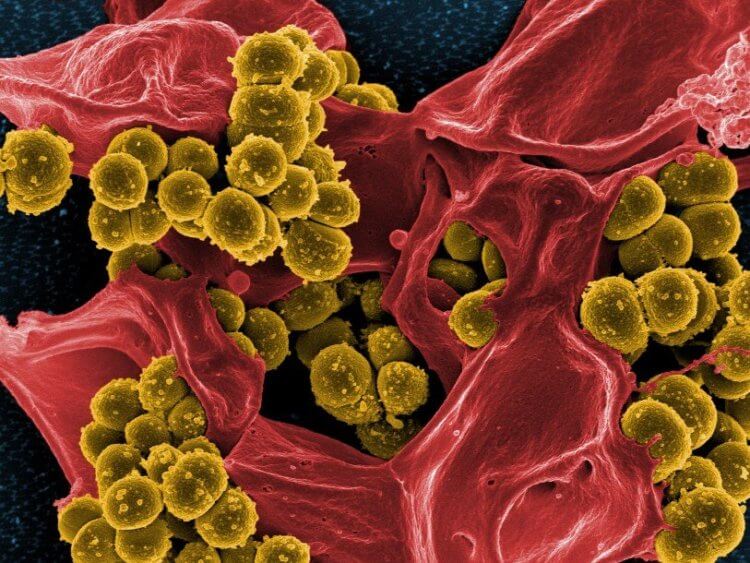
ДНК-сети эффективны против штамма золотистого стафилококка, который невосприимчив к антибиотикам
Это может объяснять тот факт, что люди с аутоиммунными заболеваниями особенно чувствительны к стафилококковым инфекциям. Судя по всему, организм не в силах с ним бороться по причине повышенного содержания S100A9. Белок попросту блокирует способность нейтрофилов создавать антибактериальные сети и приманивать к ним макрофаги. Как вы видите, иммунитет — крайне сложная система, которая порой удивляют. Некоторые ученые даже считают, что иммунитет способен подстраиваться под условия жизни, что позволяло выжить древним людям.
Возможно, после данного исследования ученые смогут создать препарат, который сможет понизить активность S100A9, чтобы стимулировать иммунитет эффективно бороться с бактериальными инфекциями. По сути, стимуляция мощного иммунного ответа — это единственный эффективный способ лечения некоторых инфекций, которые невосприимчивы к антибиотикам. К таким относится и золотистый стафилококк, смертность от которого достигает 30%. Напоследок напомню, что при помощи иммунотерапии ученые планируют бороться не только с золотистым стафилококком, но и онкологией. Правда, для лечения рака применяются другие технологии, о которых я рассказывал ранее.
